
- Химические вещества
- Химическое превращение веществ
- Периодическая система химических элементов Д.И. Менделеева
Химия - это одна из естественных наук, которые помогают нам узнавать много нового об окружающем мире и природе вещей. Помимо химии в список таких наук входят также физика и биология. Биология рассматривает и анализирует существование живых существ и организмов, а также растений и жизнь человека. Физика - это естественная наука о явлениях, происходящих вокруг нас в природе, и описывающая наиболее общие законы протекания этих явлений природы.
Химия же изучает вещества и их свойства.
Химические вещества
Вещество - это то, из чего состоит каждое тело вокруг нас. Например, молоток сделан из железа, в наших окнах есть стекла, одноразовые пакеты состоят из полиэтилена и т.д. Но есть тела, которые могут состоять из нескольких разных веществ, как, например, наш компьютер. Но все таки это определение применимо в большей степени к твердым веществам. Но мы же знаем, что помимо твердых веществ, еще существуют жидкие и газообразные, поэтому более точным будет такое определение:
Вещество - это одна из форм материи, состоящая из частиц, имеющих собственную массу (молекулы, атомы и ионы).
Другая форма материи называется полем и с его помощью частицы вещества взаимодействуют друг с другом. Изучением поле занимается физика, а получением веществ и их превращениями занимается химия.
Химическое превращение веществ

Превращение веществ бывают физическими и химическими.
Физическим превращением веществ может являться плавление веществ, когда твёрдое агрегатное вещество переходит в жидкое с сохранением этого же состава вещества, газообразование или кристаллизация, когда жидкое вещество превращается в твёрдое. Также физическим превращениям является изменение формы. Мы можем разрезать какое-то вещество на несколько частей, и оно изменит форму. Но там состав при этом не меняется.
При химическом превращения состав вещества начинает меняться. Разберем, какие бывают химические превращения.
Реакция присоединения
Первый вид химического превращения - это присоединение, когда соединяются два простых вещества отдельных по составу и образуется сложное.
Примером может являться окисления магния и получение в результате оксида магния:
2Mg+O2=2MgO
Реакция разложения
В этом варианте изначально имелось сложное вещество и образовалось два простых или больше. Примером такой реакции является разложение оксида ртути на ртуть и кислород.
2HgO=2Hg+O2
Реакция замещения
Например, замещение меди железом в растворе сульфата меди
CuSO4+Fe=FeSO4+ Cu
Реакция обмена
Обмен происходит тогда, когда у нас есть два сложных вещества, и при их взаимодействии образуются два других сложных вещества. Примером может служить йодид натрия и нитрат свинца. В результате такой реакции образуется йодид свинца и нитрат натрия.
2NaI+Pb(NO3)2=2NaNO3+PbI2
Гидролиз
Гидролиз - это частный случай реакции обмена. Здесь одним из изначальных двух сложных веществ является вода. Примером может служить разложение хлорида аммония под действием воды на гидроксид аммония и хлорную кислоту.
NH4Cl=NH4OH+HCl
Реакция нейтрализации
Это реакция кислоты с основанием, в результате которой образуется соль и вода. Примером этой реакции может служить реакция хлорной кислоты и гидроксида натрия. В результате здесь образуется соль натрий хлор и вода.
HCl+NaOH=NaCl+H2O
Периодическая система химических элементов Д.И. Менделеева
В 19 веке Менделеев Д.И. взял все вещества и выстроил их в ряд относительно заряда ядра. У каждого следующего элемента находятся разное количество протонов в ядре. Сначала он поставил элемент водород, у которого всего лишь один протон в ядре, затем гелий, у которого два протона в ядре и так далее.
Через какое-то время он заметил, что свойства этих веществ повторяются с определенной периодичностью, и решил сделать таблицу, в которой все вещества с повторяющимися свойствами находились друг под другом.
Давайте посмотрим, какая таблица получилась у Менделеева.
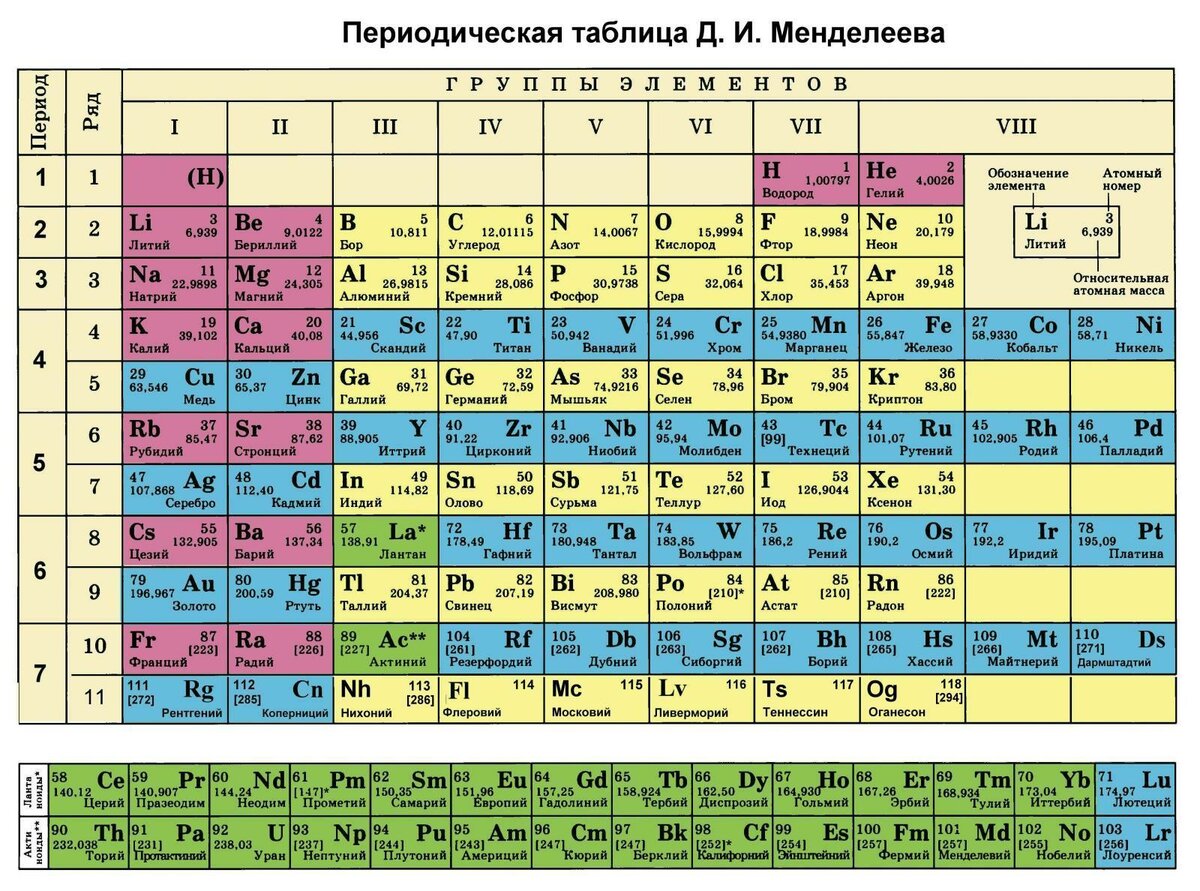
Горизонтальные линии в таблице - это периоды. Мы знаем, что у нас атом состоит из ядра и электронных оболочек. Период равен количеству этих электронных оболочек. То есть у элементов в одном периоде одинаковое количество электронных оболочек.
Мы сказали, что у атомов в одном периоде одинаковое количество электронных слоев, но количество протонов увеличивается, увеличивается, заряд ядра, и соответственно, количество электронов в атоме также увеличивается.
Следовательно, с увеличением номера элемента в периоде больше концентрация электроном и они всё с большей силой притягиваются к ядру. Это значит, что радиус атома уменьшается. Также это, значит что у них увеличивается электроотрицательность (способность притягивать электроны, окислять), а способность отдавать электроны (восстановительное свойство) уменьшается.
Вертикальные линии обозначают группы. Существуют подгруппы А и Б. В этих подгруппах у элементов немного разные свойства. Давайте посмотрим, какие это свойства.
В группе количество протонов также увеличивается, то есть увеличивается заряд ядра. Число электронов также изменяется, но при этом увеличивается количество электронных слоев, а значит сила притяжения электронов уменьшается.
Таким образом, уменьшается электроотрицательность (способность притягивать электроны, окислять), а способность отдавать электроны (восстановительное свойство) увеличивается.
Если провезти диагональ в таблице Менделеева от Бора до Полония, то все элементы, которые будут находиться ниже и левее этой диагонали будут металлами, а те элементы, которые будут находиться выше и правее - будут неметаллами. О свойствах металлов и неметаллов мы поговорим немного позднее.



Добавить комментарий